Классификация БА (2002)
Бронхиальная астма — это хронический воспалительный процесс бронхиальной стенки, вызывающий повышенную реактивность дыхательных путей, предрасполагающую к бронхоспазму в ответ на различные раздражители БА характеризуется периодическими приступами удушья или затруднения дыхания в результате бронхиальной обструкции.
Воспаление при аллергической астме носит характер аллергического антигенспецифического, а неспецифическая гиперергическая реакция в ответ на раздражения, имеющая не аллергический характер, может возникнуть только на сенсибилизированном фоне
При аллергической бронхиальной астме
- Продукция цитокинов Тх2-зависимого профиля представляет важнейшее звено
- между активацией тучной клетки,
- развивающимся в дыхательных путях аллергическим воспалением
- последующими клиническими проявлениями астмы.
Распространенность БА
- по обобщенным результатам исследований ISAAC (International Study of Asthma and Allergy in Childhood) (1998), проведенным в 56 странах мира, составляет от 1,0% до 30,8%
- Распространенность БА у детей составляет от 0,2% до 5,4%. Причем, в экологически неблагоприятных регионах Казахстана в структуре БА от 39,6% до 52% — астма тяжелого течения
- Среди взрослых в РК – 1,7% – 3,5%
Формирование конституциональных типов и клинико-патогенетических вариантов атопических заболеваний (В.И. Пыцкий, 2005)
 Предрасположенность к БА
Предрасположенность к БА
- наличие атопических заболеваний у родителей и ближайших родственников
- способность к повышенному синтезу IgE;
- функциональная, а нередко и количественная недостаточность Тх1;
- низкая продукция g-интерферона лейкоцитами;
- гиперпродукция ИЛ-5 лимфоцитами
- способность клеток-мишеней отвечать на контакт с аллергеном повышенной секрецией гистамина, лейкотриенов, простагландинов, других медиаторов аллерги
- недостаточность b2-адренорецепторов тучных клеток, эозинофилов, лимфоцитов.
Семейный анамнез
- Риск развития заболевания БА
- при отсутствии атопии у родителей — от 0 до 20%;
- При наличии атопии у матери (эффект Carter’a) -38%
- При наличии атопии у отца – 25%
- У двух родителей — до 60-100%.
Реализация генетической предрасположенности
- Основными вирусами-кандидатами на участие в этиологии и патогенезе БА являются РС-вирус, аденовирусы, вирусы парагриппа, риновирусы
- Сочетание респираторных вирусов с ингаляционными аллергенами индуцирует аллергическую сенсибилизацию значительно быстрее, чем эти факторы в отдельности
- Неадекватно низкая антигенная стимуляция -теория «замарашек»
- Чрезмерная антигенная нагрузка в период становления иммунной системы
- Экологические факторы – загрязнение воздуха
- Бытовые аллергены – экология жилища
Морфологические признаки аллергического воспаления при БА
- повышенное содержание слизи и экссудата в просветах бронхов и бронхиол вплоть до их обтурации, деструкция и/или десквамация покровного цилиндрического реснитчатого эпителия, его атрофия и плоскоклеточная метаплазия;
- утолщение подэпителиального соединительнотканного ретикулярного слоя, расширение бронхиальных микрососудов с застоем крови, отек интерстиция, увеличение массы гладких мышц бронхов, рост объема желез, секретирующих слизь;
- воспалительная клеточная инфильтрация, для которой типично присутствие эозинофилов и продуктов их секреции, тучных клеток, макрофагов, активированных Т-лимфоцитов.
Критерии тяжести астмы
| легкое | средней тяжести | тяжелое | |
| частота дневных приступов или эквивалентов | не чаще 1-2 раза в неделю | не чаще 1 раза в день | ежедневно |
| частота ночных приступов или эквивалентов | не чаще 1-2 раза в месяц | не чаще 1 раза в неделю | 2-7 раз в неделю |
| ОФВ1 и/или ПОС выд | > 80% | 80-60% | <60% |
| суточные колебания ОФВ1 и/или ПОС выд | <20% | 20-30% | >30% |
| бесприступные периоды | длительные — месяцы | недели | нет |
| обращение за неотложной помощью | нет | 1-2 раза в год | 3-6 раз в год |
Хорошо контролируемая астма (well controlled asthma) должна соответствовать следующим критериям:
- минимальное число дневных эпизодов бронхообструкции (менее 1 эпизода в сутки);
- полное отсутствие ночных симптомов (по крайней мере, менее 1 эпизода в неделю);
- нормальная переносимость физической нагрузки;
- потребность в b-агонистах короткого действия – не более двух ингаляций в сутки;
- отсутствие обращений за неотложной помощью;
- суточная лабильность бронхов – менее 20%;
- среднесуточное значение пиковой скорости выдоха – более 80%;
Критерии тяжести приступа БА
- Приступ купируется спонтанно
- Приступ купируется антигистаминным препаратом
- Купируется ингаляцией бета-миметика
- Не купируется полностью даже 3 дозами бета-миметика в течение часа (или более 6 доз в сутки) – затянувшийся приступ
- Статус астматикус
Лечение тяжелого приступа БА
| первые 30 мин | b-миметик каждые 20 мин |
| ГКС системно если больной стериодзависимый | |
| кислород | |
| 40-120 мин | |
| ОФВ1 50-70% | преднизолон 30-60 мг в\в, кислород, b-миметик |
| ОФВ1 <50% | метилпреднизолон 60-120 мг, b-миметик |
| 120-180 мин
ОФВ1 >70% |
ГКС системно 30-60 мг + эуфиллин 2,4% 10 мл в\в на физ р-ре или b-миметики (можно пролонгированные) |
| или per os до 40 мг коротким курсом — 3-5 дней+ пролонгированные b-миметики или эуфиллин | |
| ОФВ1 <70% | повторять метилпреднизолон до 300-400 мг/сут и больше + эуфиллин 2,4% 10 мл в\в, кислород, ингаляционный b-миметик каждый час — ПИТ |
Действие ГКС
- ГКС снижают число циркулирующих в крови базофилов, эозинофилов, моноцитов и лимфоцитов за счет ингибиции факторов, стимулирующих гранулопоэз
- ГКС стимулируют синтез нейтрофилов в костном мозге и таким образом повышают их содержание в периферической крови
- ГКС ингибируют приток нейтрофилов, эозинофилов, лимфоцитов в очаг воспаления
- нарушают функциональную активность лейкоцитов, тучных, эндотелиальных клеток и фибробластов
- угнетают продукцию и действие гуморальных факторов, вовлеченных в воспалительный процесс
- Угнетают синтез ИЛ-1, ИЛ-6, aTNF, ИЛ-8, ИЛ-5
- ГКС блокируют синтез не только цитокинов, но и цитокиновых рецепторов
- ГКС вызывают апоптоз ИКК.
- ГКС с одной стороны стимулируют апоптоз эозинофилов через активацию FasL, с другой стороны уменьшают высвобождение цитокинов с противоположным действием
топические кортикостероиды 2-го поколения – будесонид, флюнисолид, флутиказон
Нет системных побочных эффектов
Удобство применения и дозировки
более эффективно
–тормозят миграцию и пролиферацию Т-лимфоцитов,
–тормозят секрецию CD4 цитокинов, уменьшают выброс гистамина,
–экспрессию адгезивных молекул,
–стимулируют апоптоз CD3+, CD4+, CD8+ CD25+ лимфоцитов, тучных клеток и эозинофилов в ткани легких больных БА
При тяжелом течении БА в лечении больных не обойтись без кортикостеороидов
но их применение может усугубить недостаточность Тх1-типа иммунного ответа и усугубить иммунные нарушения при БА
Повышает риск инфекции, а инфекция провоцирует обострение БА
При тяжелом течении БА может развиться стероидрезистентность – из-за:
- Ремоделирования бронхиальной стенки
- Снижения чувствительности и количества рецепторов к ГКС
Иммунотерапия БА
СИТ – лечение аллергенами
Иммунопрепараты – подавление Тх2 и стимуляция Тх1
–Естественными антагонистами Тх2-зависимых цитокинов являются цитокины Тх1 профиля
–Антагонисты цитокинов (ИЛ-4 и ИЛ-5)
–Блокирования реакции антигенпредставляющих клеток с Тх2-лимфоцитами, предотвращающими их активацию
–Блокада IgE
Стимуляция Тх1
- Альфа-интерферон
- Гамма-интерферон
- Рибомунил
- Полиоксидоний
- Бронхомунал
- Гистаглобулин
- Тимические факторы – тималин, Т-активин, вилозен и др.
Эффекты интерлейкина-2
42 ребенка
Бронхиальная астма тяжелого течения
из 42 детей 11 – гормонозависимые (26,2%)
Возраст от 2,5 до 7 лет (средний возраст – 4,35±1,26 лет)
Госпитализация в экстренном порядке в астматическом статусе
с дыхательной недостаточностью I степени — у 27 детей
II степени – у 15 детей
Ронколейкин
250-500 тыс. МЕ с интервалом 48 часов
п/к или ингаляционно
4 введения
на 4-14 день после госпитализации
Кортикостероиды в/в капельно
Эуфиллин, тиосульфат натрия, кислород
Антибактериальная и антигрибковая терапия
Муколитики
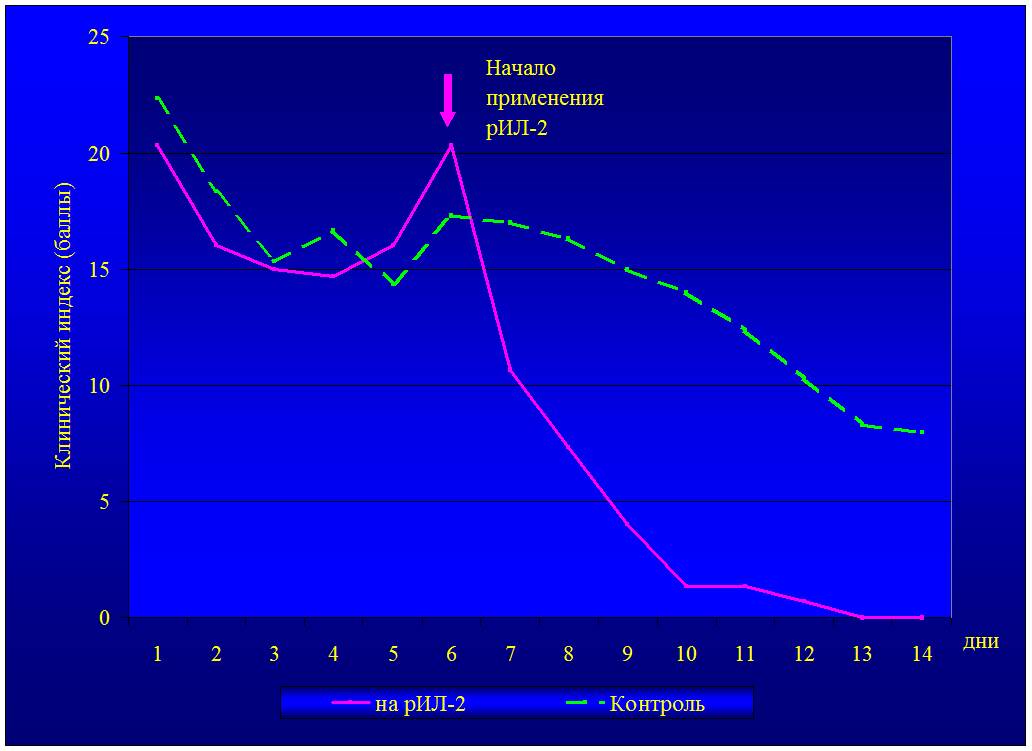
Динамика клинических симптомов у детей
В результате применения рИЛ-2
- Произошла быстрая и стойкая нормализации состояния больных детей и купирование обострения
Что позволило снять гормонозависимость (2 детей с КС перешли на тайлед; 3 с пероральных и на ингаляционые КС)
Нормализовались показатели иммунного статуса, произошла стимуляция Тх1-зависимого ответа
Произошла стимуляция противовирусного иммунитета
Снизилось число эпизодов ОРВИ
Снизилось число обострений и их тяжесть, реже требовалась госпитализация
Улучшился ответ на базисную терапию
Бронхиальная астма из трудноконтролируемой (brittle-астма) перешла в разряд контролируемой базисными препаратами (кромогликатом или ингаляционными КС)
Повторный курс – 6 детей через 1 год
Показания для 2-го курса:
- Снижение эффективности базисной терапии – неконтролируемая астма
- Повышение потребности в β-миметиках, учащение дневных и ночных симптомов, несмотря на повышение ступени базисной терапии
- Учащение эпизодов ОРВИ
Рандомизированное двойное слепое
плацебо-контролируемое исследование
Ронколейкина во время СИТ
Поллиноз с клиническими проявлениями риноконъюнктивита, сенной астмы и пыльцевой интоксикации
33 больных получили рИЛ-2 и 18 — плацебо
Возраст от 18 до 45 лет
Ронколейкин
250 тыс. МЕ с интервалом 72 часа
п/к
4-5 введения
на 10-10-10-11 разведениях аллергенов при начальном разведении 10-20
Изменение абсолютного содержания лимфоцитов основных популяций при применении рИЛ-2+СИТ
Рандомизированное двойное слепое
плацебо-контролируемое исследование
Ронколейкина во время обострения поллиноза
Поллиноз с клиническими проявлениями риноконъюнктивита, сенной астмы и пыльцевой интоксикации
30 Больных получили рИЛ-2 14 — плацебо
Возраст от 18 до 45 лет
Ронколейкин
250- 500 тыс. МЕ с интервалом 48-72 часов
п/к
3-5 введения в разгар сезона обострения
Изменение относительного содержания лимфоцитов основных популяций при применении рИЛ-2 в период обострения
Динамика клинических симптомов за 14 дней госпитализации (в баллах)
Число эпизодов ОРЗ и ОРВИ за 12 мес
(на одного больного)
выводы
Комплексная терапия (СИТ+рекомбинантный ИЛ-2) приводит к снижению интенсивности и сокращению длительности периода обострения.
У больных, получавших рекомбинантный ИЛ-2 при обострении поллиноза, клиническая эффективность выражалась в быстром купировании симптомов заболевания, достоверным повышении функции внешнего дыхания (уменьшения обструкции по данным спирографии), повышением качества жизни,
У больных наблюдалось снижением числа простудных заболеваний и количества обострений сопутствующих хронических заболеваний в течение года.
При полном положительном эффекте применения рекомбинантного ИЛ-2 у больных отмечалась нормализация показателей иммунного статуса с повышением уровня экспрессии CD25.